미생물 세포공장 대사조절 기술의 개발동향

경상대학교 김선원 교수
1. 개요
합성생물학 기술의 발달로 기존 대사공학 기술로 구현이 힘들었던 대사경로 흐름의 역동적 조절(dynamic regulation)이 가능해졌다. 대사흐름의 다양한 역동적 조절은 일련의 대사중간체 감지기와 유도인자(metabolite sensors and inducers)들에 의해서 전사, 번역, 번역후 수식단계(transcriptional, translational and posttranslational levels)에서 진행된다. 이들 각 단계에서의 역동적 대사조절은 상이한 반응시간척도(different dynamic time-scales)를 갖는 다양한 대사조절 장치들에 의해서 이루어지고, 다양한 돌발변수들이 공존하는 산업현장에서의 적용을 위해서는 이들 대사조절회로의 견고성(robustness)이 중요한 특성이 된다.
합성생물학은 신속하고 저렴한 유전자 합성 및 분석기술의 발달로 바이오부품의 설계-제작-시험을 통한 유전자회로에 대한 이해와 산업화 가능성을 제고하고 있다. 산업균주 개발에 성공하기 위해서는 수율(yield), 농도(titer), 생산성(productivity)의 3가지 중요한 인자를 반드시 고려해야 한다. Van Dien은 $1.00/lb 가격수준의 대량생산 생물제품의 생산성 기준으로 수율은 최대 이론수율의 80%, 생산농도는 50 g/L, 생산성은 3 g/(L h)를 제시하고 있다. 상기 3가지 인자는 서로 상충되는 개념으로 특히 수율과 생산성은 상호절충(trade-off)의 관계에 있다(그림 1). Zhuang들은 생산균주 설계에서 수율을 최적화한 경우에 생산성은 감소하는 상호간의 내재적 절충관계를 보고하였다[2]. 대사공학은 대부분의 경우에 목적산물 생합성경로만을 염두에 두고 극대화하기 때문에 균체생육에 필요한 대사자원들이 부족으로 균체증식과 산물생산이 상호절충(trade-off)되는 결과를 갖고 온다(그림 2). 따라서 생산수율을 향상만을 염두에 둔 대사조절 전략들은 생육속도 감소로 인한 체적 생산성(volumetric productivity)의 감소롤 귀결된다. 낮은 체적 생산성은 설비투자비 및 운영비 부담의 증가로 산업화의 제약요인이 된다.
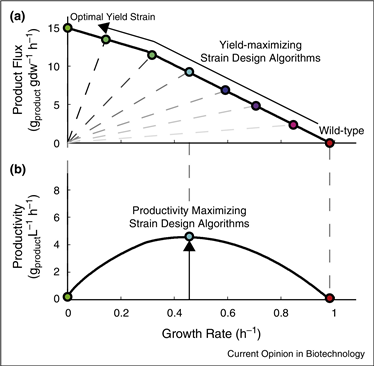
그림 1. 균주 설계 알고리듬: 균주설계는 대부분 생산성 보다는 수율향상에 중점을 두고 있다. 생육속도를 희생하면서 생산수율을 증가시키는 유전자 조작들이 진행된다(a, solid arrow). 이러한 균주조작들은 static techniques (static gene overexpression or deletion)을 통해서 진행이 되기 때문에 목표 대사경로의 dynamic control은 없다. 그러나 최근에 dynamic flux balance analysis (dFBA)에 기반을 둔 생산성을 고려한 균주 설계 알고리듬이 개발되고 있다. 이 알고리듬은 product flux와 growth rate를 설정하고 이론적으로 균주를 설계한다(a, dots). 그리고 productivity, yield, titer를 목적변수로 해서 균주를 최적화 한다(b).
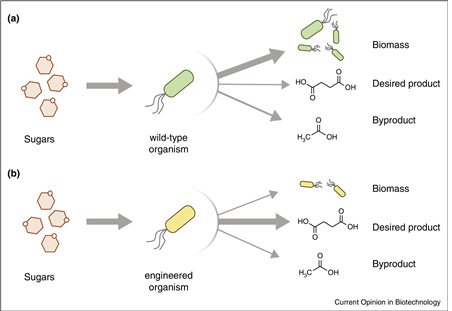
그림 2. 야생형균주와 재조합균주의 기질 분배: 각 산물들로의 상대적인 기질흐름의 양은 화살표의 굵기로 표시함. (a) 야생형균주에서 대사흐름은 바이오매스로 대부분 흐르고 목적산물과 부산물로는 제한된 적은 양만이 흐름. (b) 재조합균주에서 대사흐름은 목적산물로 주로 가도록 대사 재설계됨. 대사흐름의 최대한도가 기질 유입속도에 의해서 제한되어지기 때문에 바이오매스와 목적산물로의 대사흐름은 내재적인 trade-off의 관계에 있음.
2. 이단계 능동적 대사조절(two-stage dynamic control strategy)
산물 생합성경로 강화로 인한 생육속도의 심각한 감소문제를 해결하기 위해서 생육단계(growth stage)와 생산단계(production stage)로 구분해서 대사경로를 조절하는 이단동적조절(two-stage dynamic control) 방식을 적용할 수 있다. 생육단계에서는 산물 생합성경로 강화 유전자들의 발현을 억제해서 전체 대사흐름이 야생형 균주와 유사하도록 해서 생육속도를 향상시키고, 일정한 균체농도에 도달하면 생산단계로 전환해서 산물 생합성경로 강화 유전자들의 발현을 통해서 생산성을 극대화하는 것이다[3, 4]. 동적 대사조절(dynamic control)의 이익을 분석하기 위해서 정적 대사조절(static control strategy)와 동적 대사흐름 균형 분석(dynamic flux balance analysis)에 의한 이단동적조절(two-stage dynamic control strategy)의 생산성을 비교한 결과 동적조절전략(dynamic control strategy)이 생산성을 대폭 향상시키는 것을 알 수 있다(그림 3). 이러한 동적대사조절은 최근 합성생물학의 발전으로 유전자회로를 이용한 대사경로의 핵심 효소들의 발현 및 대사흐름을 연속적이면서 역동적으로 조절을 할 수 있는 수준으로까지 발전하였다.
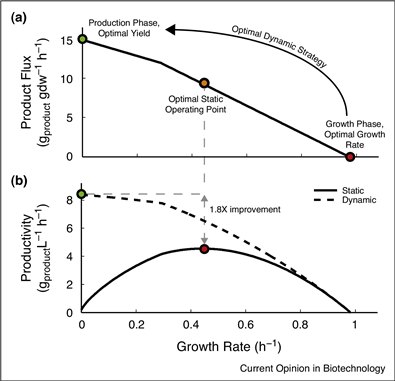
그림 3. 생산성 향상을 위한 정적(static) 및 동적(dynamic) 대사공학(metabolic engineering) 전략의 비교. (a) 숙신산 생산을 위한 생산성 한계. (b) static strategy (solid line)와 dynamic strategy (dashed line)에 따라 설계된 균주들의 한계 생산성 비교. Specific product flux와 growth rate로 생산균주의 hypothetical operating points을 production envelope 곡선(a, solid line)에서 선택함. Static strategy의 생산성은 dynamic gene regulation이 없는 single-stage fermentation 조건으로 모사. Dynamic strategy는 wild-type growth rates를 갖는 growth stage와 hypothetical strain의 product fluxes를 갖는 production stage로 구성되는 two-stage fermentation을 의미함.
3. 대사물질 감지(metabolite sensor) 기반 연속조절 유전자회로
연속대사조절(continuous metabolic control)은 세포 내부 및 외부의 환경변화를 동적으로 감지하고 변화된 환경에 맞춰서 대사를 조절하는 것으로 산업현장의 불균일한 조업환경과 매번 동일하지 않은 발효조건들에 맞춰서 세포공장이 능동적으로 대응하게 함으로써 목적산물의 생산성이 항상 극대화 되도록 하는 것이다. Farmer & Liao가 라이코펜 생산성 향상을 목적으로 이러한 능동적 연속조절 유전자회로를 최초로 사용하였다. 이들은 acetyl phosphate-activated sensor를 개발해서 해당경로의 대사흐름을 감지하고 해당경로 대사흐름에 맞게 라이코펜 생합성경로 발현을 조절하는 유전자회로를 구축해서 생산성을 획기적으로 향상시켰다(그림 4a). 연속조절 유전자회로의 핵심인 다이내믹 센서(dynamic sensors)는 핵심 대사중간체에 민감하게 반응하는 발현 프로모터들을 전사체 분석을 통해서 얻고 이들을 생합성경로 발현조절에 접목함으로써 구축될 수 있다(그림 4b). 그러나 연속조절 유전자회로의 다이내믹 센서와 구동자(actuator)를 목적물질이 변경될 때마다 다시 개발해야 되기 때문에 많은 시간과 자원의 투입이 요구되는 단점이 있다.
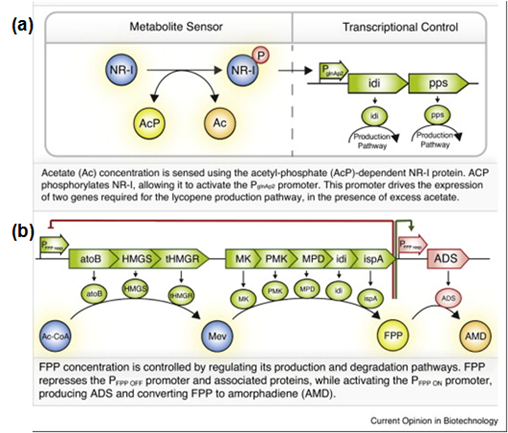
그림 4. Dynamic control 구현을 위한 유전자회로. (a) acetyl phosphate-activated sensor 기반의 라이코펜 생합성 유전자회로. (b) FPP-activated sensor 기반의 아모파디엔 생합성 유전자회로.
4. 고찰
최근 합성생물학의 진보로 대사흐름을 다이내믹하게 조절하는 능동적 대사공학(dynamic metabolic engineering)이 주목을 받고 있다. 이를 통해서 발효공정의 3대 핵심인자인 생산수율(yield), 산물농도(titer), 생산성(productivity)을 획기적으로 향상시킬 수 있다. 대사흐름을 조절하기 위해서 동적되먹임조절(dynamic feedback control)에 기반을 둔 대사물질 감지(metabolite sensor) 연속조절과 이단계생육조건(two-stage growth conditions)에 기반을 둔 이단계 능동적 대사조절(two-stage dynamic control strategy)은 능동적 대사공학의 중요한 핵심기술이다. 상기 두 핵심 기술은 목적산물의 생산성(productivity) 뿐만 아니라, 수율(yield)과 농도(titers)도 더불어 향상 시킬 수 있다. 동적대사조절전략(dynamic control strategies)이 더 효율적이고 광범위하게 이용되기 위해서는 두가지 중요한 발전이 요구된다. 첫째는 유전자 회로가 견고해서 균주와 발효조건에 상관없이 일정한 성능을 나타내야 한다. 두 번째는 연속조절에서 감지(sensing)와 구동(actuation)의 역동성(dynamics)이 대사흐름을 효율적으로 조절할 수 있을 정도로 충분히 빨라야 한다. 향후에 합성생물학의 발전은 이런 문제들을 해결하고 대사공학과 생물공정에서 동적조절의 활용의 폭을 넓힐 것이다. 본 동향원고는 Venayak et al. (2015)의 “Engineering metabolism through dynamic control”에 기반하고 있음.
5. 참고문헌
1. Van Dien S: From the first drop to the first truckload: commercialization of microbial processes for renewable chemicals. Curr Opin Biotechnol 2013 http://dx.doi.org/10.1016/j.copbio.2013.03.002.
2. Zhuang K, Yang L, Cluett WR, Mahadevan R: Dynamic strain scanning optimization: an efficient strain design strategy for balanced yield, titer, and productivity. DySScO strategy for strain design. BMC Biotechnol 2013, 13:8..
3. Gadkar KG, Doyle Iii FJ, Edwards JS, Mahadevan R: Estimating optimal profiles of genetic alterations using constraint-based models. Biotechnol Bioeng 2005, 89:243-251.
4. Anesiadis N, Cluett WR, Mahadevan R: Dynamic metabolic engineering for increasing bioprocess productivity. Metab Eng 2008, 10:255-266.
5. Farmer WR, Liao JC: Improving lycopene production in Escherichia coli by engineering metabolic control. Nat Biotechnol 2000, 18:533-537.
6. Dahl RH, Zhang F, Alonso-Gutierrez J, Baidoo E, Batth TS, Redding-Johanson AM, Petzold CJ, Mukhopadhyay A, Lee TS, Adams PD et al.: Engineering dynamic pathway regulation using stress-response promoters. Nat Biotechnol 2013, 31:1039-1046.
7. Venayak N, Anesiadis N, Cluett WR, Mahadevan R.: Engineering metabolism through dynamic control. Curr Opin Biotechnol. 2015, doi: 10.1016/j.copbio.2014.12.022.





