진세노사이드를 이용한 뇌인지기능 향상에 대한 연구

한국과학기술원 한진희 교수
1. 개요
인삼(ginseng)은 동양권 국가에서 수천 년 전부터 민간 의약으로 사용되어 오고 있다. 인삼의 의학적 사용은 기원전 33년의 고대 중국 문헌 기록에서도 언급이 되어있으며, 한국에서 자라는 Panax ginseng, 중국에서 자라는 Panax notoginseng, 미국 대륙에서 발견되는 Panx quinquefolium 등의 다양한 인삼 종이 존재하고 있다. 인삼이 가진 여러 의학적 효능 가운데, 학습 효과와 기억력 향상에 가지고 있는 효능이 주목되었으며 최근에는 여러 실험적, 임상적 시도를 통하여 인삼이 가지는 기억력 향상 효과에 대한 연구가 진행되어 오고 있다. 앞선 연구를 통하여 기억력 향상 효과에 기여하는 인삼 주 성분으로 진세노사이드(ginsenoside)라는 화합물이 연구의 주 대상으로 주목받았다. 진세노사이드는 인삼의 주요 약리효과를 나타내는 Dammarane-type Triterpene Saponins의 특징을 가지는 천연화합물로 180종 이상의 진세노사이드가 알려져 있다 (그림 1). 진세노사이드는 인삼에 함유되어 있는 양에 따라 메이저, 마이너 진세노사이드로 나뉘는데, 이 중 메이저 진세노사이드에 해당되는 Rg1, Rb1 등의 진세노사이드는 기억력 향상의 효과가 있음이 실험적으로 입증되었다 (Mook-Jung et al. 2001).
노화 (Senescence), 알츠하이머 (Alzheimer's disease) 등의 원인으로 나타나는 치매는 신경 퇴행성 뇌질환의 일종으로 현대 사회의 주요 질환 중 하나로 분류될 만큼 중요한 사회적 문제로 고려되고 있다. 치매의 여러 증상 중 가장 중요한 것은 기억력 감퇴 및 인지 기능 저하이다. 치매의 원인과 치료 방법에 대한 연구가 활발히 진행 중이지만, 아직까지 명확환 원인의 규명과 확실한 치료 방법이 밝혀지지 않은 상황이다.
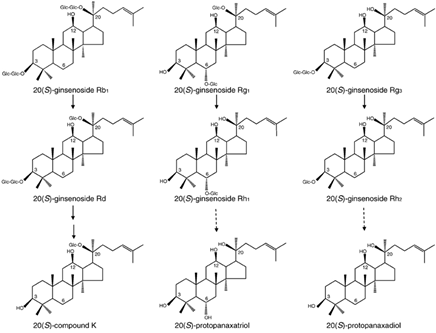
그림 1 진세노사이드의 종류
진세노사이드는 인삼 내 함유량에 따라 메이저/마이너 진세노사이드로 나뉜다. 함유량이 95% 이상인 Rb1, Rd, Rg1 등이 메이저 진세노사이드로 분류되며 실제 인삼에서는 마이너 진세노사이드로부터 메이너 진세노사이드로 생합성 되어 저장된다.
그 중 학습과 기억에 대한 진세노사이드의 약리 효과를 연구하는 여러 연구팀에서는 몇몇 종류의 진세노사이드가 치매 질환의 진행을 늦추고 치매에 의한 인지 기능 저하 현상을 회복시킬 수 있다는 연구 결과를 발표하고 있다. 해당 연구 결과들은 진세노사이드가 치매 진행 억제에 갖는 생리학적 효과, 치매 모델 실험동물에서 보이는 인지 기능 회복 효과들을 보여주고 있다. 따라서 본 보고서에서는 여러 신경 퇴행성 질환 모델에서 나타나는 진세노사이드의 치료 효과에 대한 실험적 결과들을 중심으로 진세노사이드의 약리 효과 규명에 대한 연구 동향에 대해 고찰해 보고자 한다.
2. 진세노사이드가 치매 모델에서 보이는 약리 효과
진세노사이드가 치매 치료에 보이는 효과를 연구하기 위하여 최근의 연구에서는 치매 환자에서 나타나는 생리학적 현상을 모방할 수 있는 여러 치매 모델 시스템 (세포주 또는 실험동물)을 활용하였다. 이러한 모델 시스템들은 대부분 아밀로이드(Amyloid) 단백질의 플라크 형성을 유도하고 있는데, 아밀로이드 플라크 형성은 대부분의 치매 환자들의 뇌 조직에서 발견되며 신경 세포의 손상을 일으켜 치매의 주요 증상들을 일으키는 주 원인으로 지목되고 있다. 한 연구에서는 난소 적출(Ovariectomized) 쥐에 D-galactose를 주입하여 아밀로이드 단백질의 발현이 증가한 치매 모델 쥐를 생산하고, 이 모델에 진세노사이드 Rg1을 6주 간 투여하여 치매 증상에 미치는 영향을 관찰하였다.
그 결과, 진세노사이드 Rg1을 투여한 쥐에서 아밀로이드 단백질의 양이 감소하고 손상되었던 공간
기억 능력이 회복되는 것을 관찰할 수 있었다 (그림 2,3 X. Zhang et al. 2012).
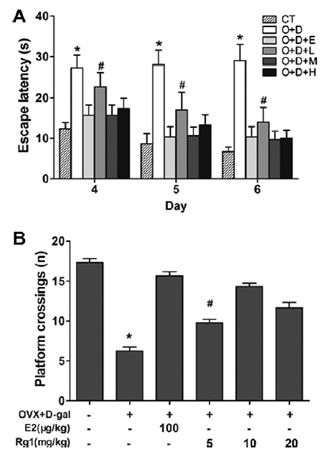
그림 2 치매 모델에서 진세노사이드 Rg1에 의한 공간 기억 회복.
공간 기억에 대한 실험적 검증 방법인 Morris water maze 실험에서 Rg1을 투여한 그룹(O+D+L/+M/+H)이 Rg1을 투여하지 않은 치매 모델 그룹(O+D)과 비교하였을 때, 대조군(CT)에 근접한 공간 기억 능력을 보여주고 있다. (X. Zhang et al.2012)
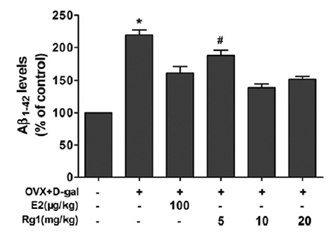
그림 3 치매 모델에서 진세노사이드 Rg1에 의한 아밀로이드 단백질 형성 억제 Rg1을
투여한 그룹이 Rg1을 투여하지 않은 치매 모델 그룹과 비교하였을 때
더 낮은 아밀로이드 단백질 수준을 보이고 있다. (X. Zhang et al. 2012)
같은 연구에서 진세노사이드 Rg1의 투여는 아밀로이드 전구체를 분해하여 아밀로이드 플라크 형성을 촉진시킬 수 있는 BACE 1 효소의 발현을 감소시키는 것을 확인하였다. 이와 관련하여 2012년 Li-min Chen 팀에서는 amyloidogenesis의 in vitro 모델로 사용되는 N2a-APP695 세포주에 Rg1을 처리하였을 때, BACE 1 프로모터에 결합하여 BACE 1 유전자 전사를 억제시키는 PPARγ가 세포질로부터 핵으로 이동하여 BACE 1의 유전자 발현 수준을 감소시키는 것을 관찰하였다. 결과적으로 이는 아밀로이드 단백질의 플라크 형성을 감소시켜 진세노사이드 Rg1에 의하여 알츠하이머 병의 증상을 완화할 수 있다는 근거가 된다.
또한, 다른 연구팀에서는 아밀로이드 단백질을 처리한 PC12 세포주에 진세노사이드 Rg1을 처리하였을 때, 젖산탈수소효소(LDH), 일산화질소(NO), 활성산소(ROS) 발생 및 세포 내 칼슘 농도 증가 등의 세포 손상 신호가 감소하는 것을 관찰하였다. 이를 통하여 진세노사이드 Rg1이 아밀로이드 플라크의 형성을 막는 것에만 관여하는 것이 아니라 아밀로이드 플라크에 의한 세포 손상을 완화하는 데에도 역할을 할 수 있다는 사실이 입증되었다 (Yue-hua Wang et al. 2009).
진세노사이드 Rg1이 아밀로이드 플라크의 형성과 이에 따른 세포 손상을 막을 수 있는 메커니즘에 관한 연구는 2012년 Chun shi 팀에 의하여 보고되었다. 진세노사이드 Rg1은 호르몬 유사물질은 피토에스트로젠 (Phytoestr -ogen)으로 알려져 있어 에스트로겐 수용체 신호전달경로를 활성화 시킬 수 있을 것으로 추측되었다. 해당 연구팀에서는 진세노사이드 Rg1의 처리가 에스트로겐 수용체를 인산화시키는 것을 확인하였으며 에스트로겐 신호전달경로 상에 있는 PKC, ERK/MAPK, PI3K/Akt등의 억제제를 투여하여 진세노사이드 Rg1에 의한 효과가 사라지는 것을 관찰함으로써 진세노사이드 Rg1의 효과가 에스트로겐 신호전달경로를 통하여 나타난다는 것을 발표하였다.
한편, SAMP8 (Senescence accelerated mouse prone 8) 노화 생쥐 모델을 이용한 연구팀에서는 3개월간의 진세노사이드 Rg1의 투여를 통해 아밀로이드 단백질의 감소, 기억력 회복과 더불어 PKA/CREB 신호전달경로의 활성화, BDNF (Brain derived neurotrophic factor)의 증가 등을 관찰하였다 (Yan-Qing Shi et al. 2010). PKA, CREB, BDNF는 여러 동물에서 장기 기억 형성에 중요한 역할을 한다는 것이 밝혀진 분자들로 위의 연구 결과를 통해 진세노사이드 Rg1이 치매 모델에서 기억력 회복 효과를 일으킬 수 있다는 것을 더욱 기대해 볼 수 있다. 이러한 PKA/CREB 신호전달경로의 활성 증가는 아밀로이드 전구체 과발현을 이용한 Fang 팀의 연구에서도 발표되었다 (Fang et al. 2012).
또한, 진세노사이드 Rg1은 아밀로이드 단백질에 의한 미토콘드리아의 역기능 및 과산화수소 노출에 의한 세포 손상 완화를 통해 세포 사멸을 억제할 수 있는 것으로 밝혀졌다. 그 외에도 진세노사이드 Rg1이 뇌의 해마(Hippocampus) 영역에서 신경전구세포의 증식과 분화를 촉진시킬 수 있다는 연구 결과들이 발견됨에 따라 진세노사이드 Rg1에 의한 신경 퇴행성 질환 치료 효과를 기대케 한다 (Cheng et al. 2005, Huang et al. 2012, Liu et al. 2011).
진세노사이드 Rg1 외에 다른 진세노사이드의 경우에도 치매 치료 효과를 보인다는 연구 결과가 있다. 아밀로이드 플라크 형성 외에 타우 (tau) 단백질의 과인산화도 알츠하이머 병의 원인으로 지목된다. 2011년 Ling Li 팀에서는 단백질 탈인산화효소의 억제제인 okacaic 산을 사용하여 타우 단백질의 과인산화를 유도한 모델에 진세노사이드 Rd를 처리한 결과, 단백질 탈인산화효소인 PP-2A의 활성을 증가시켜 타우 단백질의 과인산화를 막고 이로 인한 신경 세포의 독성을 감소시키는 것을 관찰하였다.
또한, 진세노사이드 Rg2는 과량의 글루탐산에 의한 신경세포 독성을 완화하는 역할이 밝혀졌으며 진세노사이드 Rb1, Rg3의 경우에도 아밀로이드 플라크로부터 신경세포를 보호 또는 아밀로이드 단백질 수준을 감소시키는 방식을 통해 치매 증상을 완화할 수 있다는 보고들이 있다 (Li et al. 2007, Xiaxie et al. 2010, Yang et al. 2009). 위의 여러 연구 결과들은 다양한 종류의 진세노사이드가 신경 퇴행성 질환의 하나인 치매 치료에 효과적인 약물로서 사용될 수 있음을 시사하고 있다.
3. 고찰
진세노사이드는 치매의 주 원인인 아밀로이드 단백질 플라크의 형성을 억제하고 이에 따른 신경 세포 손상을 막으며 기억 형성에 관여하는 세포 내 분자들을 활성화하여 치매 치료 약물로 활용될 수 있는 잠재력을 가지고 있다. 또한, 다른 신경 퇴행성 질환 중 하나인 파킨슨씨병 (Parkinson's disease) 모델 시스템에서도 진세노사이드의 투여가 도파민 신경세포의 사멸을 막음으로써 도파민 부족에 의한 파킨슨씨병에 치료 효과를 보일 수 있다는 연구 결과도 보고되고 있다 (Xu et al. 2009, Chen et al. 2005). 현대 사회에서 치매는 다양한 발병 원인 및 치료 약물의 부재 등으로 인하여 효과적인 치료에 난항을 겪고 있다. 치매를 포함한 여러 신경 퇴행성 질환에서 갖는 진세노사이드의 약리 효과에 관한 연구 결과들은 진세노사이드를 이용한 치매 치료에 큰 도움이 될 것으로 기대되고 있다. 앞으로는 진세노사이드가 보이는 치료 효과에 대한 실험적 연구와 함께 치매 치료에 직접적으로 활용 가능한 임상적 연구 결과들이 더해져 진세노사이드를 직접적으로 치매 치료 약물로서 활용할 수 있도록 하는 연구들이 진행될 것으로 전망된다.
참고문헌
1. Yong CHENG, Li-hong SHEN, Jun-tian ZHANG. Anti-amnestic and anti-aging effects of ginsenoside
Rg1 and Rb1 and its mechanism of action. Acta Pharmacologica Sinica. 2005, 2:143-149
2. X. Zhang, J. Wang, Y. Xing, L. Gong, H. Li, Z. Wu, Y. Li, J. Wang, Y. Wang, L. Dong and S. Li. Effects
of Ginsenoside Rg1 or 17β-Estradiol on a Cognitively Impaired, Ovariectomized Rat Model of
Alzheimer’s Disease Neuroscience. 2012, 220:191–00
3. Yan-Qing Shi, Tian-Wen Huang, Li-Min Chen, Xiao-Dong Pan, Jing Zhang, Yuan-Gui Zhu and Xiao-
Chun Chen. Ginsenoside Rg1 Attenuates Amyloid-β Content, Regulates PKA/CREB Activity, and
Improves Cognitive Performance in SAMP8 Mice. Journal of Alzheimer’ Disease. 2010, 19:977–89
4. Tianwen Huang, Fang Fang, Limin Chen, Yuangui Zhu, Jing Zhang, Xiaochun Chen, and Shirley Shidu
Yan. Ginsenoside Rg1 Attenuates Oligomeric Aβ1-42-Induced Mitochondrial Dysfunction. Curr
Alzheimer Res. 2012 3: 388–95.
5. Li-min Chen, Zhi-ying Lin, Yuan-gui Zhu, Nan Lin, Jing Zhang, Xiao-dong Pan, Xiao-chun Chen.
Ginsenoside Rg1 attenuates β-amyloid generation via suppressing PPARγ-regulated BACE1 activity in
N2a-APP695 cells. European Journal of Pharmacology 2012 675:15–21
6. Yue-Hua Wang and Guan-Hua Du. Ginsenoside Rg1 inhibits b-secretase activity in vitro and protects
against Ab-induced cytotoxicity in PC12 cells. Journal of Asian Natural Products Research 2009
11:604-612
7. Wei Li, Yanqi Chu, Lan Zhang, Linlin Yin, Lin Li. Ginsenoside Rg1 prevents SK-N-SH neuroblastoma
cell apoptosis induced by supernatant from A1–0-stimulated THP-1 monocytes. Brain Research
Bulletin 2012 88:501–506
8. Chun Shi, Dong-dan Zheng, Li Fang, Fengming Wu, Wing Hang Kwong, Jie Xu. Ginsenoside Rg1
promotes nonamyloidgenic cleavage of APP via estrogen receptor signaling to MAPK/ERK and
PI3K/Akt. Biochimica et Biophysica Acta 2012 1820:453–460
9. Qian Liu, Jun-Ping Kou Bo-Yang Yu, Ginsenoside Rg1 protects against hydrogen peroxide-induced
cell death in PC12 cells via inhibiting NF-kB activation. Neurochemistry International 2011 58:119–25
10. Fang Fang, Xiaochun Chen, Tianwen Huang, Lih-Fen Lue, John S. Luddy, Shirley ShiDu Yan. Multi-
faced neuroprotective effects of Ginsenoside Rg1 in an Alzheimer mouse model Biochimica et
Biophysica Acta 2012 1822:286–292
11. Ling Li, Juanfang Liu, Xiaodong Yan, Kefeng Qin, Ming Shi, Tian Lin, Yi Zhu, Tao Kang, Gang Zhao.
Protective effects of ginsenoside Rd against okadaic acid-induced neurotoxicity in vivo and in vitro.
Journal of Ethnopharmacology 2011 138:135–141
12. Na Li, Bin Liu, Dean E. Dluzen, Yi Jin. Protective effects of ginsenoside Rg2 against glutamate-
induced neurotoxicity in PC12 cells. Journal of Ethnopharmacology 2007 111:458–463
13. Xiaxie, Hai-Taowang, Chun-Lili, Xu-Hong Gao, Jin-Landing, Hai-Huazhao and Yong-Lilu.
Ginsenoside Rb1 protects PC12 cells against β-amyloid-induced cell injury. Molecular Medicine
REPORTS 2010, 3:635-639
14. Lingling Yang, Jianrong Hao, Jing Zhang, Wenjun Xia, Xifeng Dong, Xiaoyan Hu, Feng Kong and Xing
Cui. Ginsenoside Rg3 promotes beta-amyloid peptide degradation by enhancing gene expression of
neprilysin. JPP 2009, 61: 375–80
15. Li Xu, Wen-Fang Chen and Man-Sau Wong. Ginsenoside Rg1 protects dopaminergic neurons in a
rat model of Parkinson’ disease through the IGF-I receptor signalling pathway. British Journal of
Pharmacology 2009, 158:738–748
16. Xiao-chun CHEN, Yi-can ZHOU, Ying CHEN, Yuan-gui ZHU, Fang FANG, Li-min CHEN. Ginsenoside
Rg1 reduces MPTP-induced substantia nigra neuron loss by suppressing oxidative stress. Acta
Pharmacologicia Sininca 2005 1:56-62
17. Inhee Mook-Jung, Hyun-Seok Hong, Jung Hyun Boo, Kang Hee Lee, Sung Hwan Yun, Mi Young
Cheong, Insoo Joo, Kyoon Huh, and Min whan Jung. Ginsenoside Rb1 and Rg1 Improve Spatial
Learning and Increase Hippocampal Synaptophysin Level in Mice. Journal of Neuroscience
Research, 2001, 63:509-515
18. Shergill, Amandeep. Ginseng and Memory. Nutrition Bytes, 1998. 4: article 7





