효모 세포 내 조효소(NADPH) 생산 재설계를 통한
진세노사이드(Protopanaxadiol) 고효율 생산 대사경로 개발

한국화학연구원 김재응 박사, 이주영 박사
Jae-Eung Kim, In-Seung Jang, Bong Hyun Sung, Sun Chang Kim, and Ju Young Lee. "Rerouting of NADPH synthetic pathways for increased protopanaxadiol production in Saccharomyces cerevisiae. Scientific reports 8, no. 1 (2018): 15820.
1. 연구배경
인삼(ginseng)은 전세계적으로, 특히 아시아 국가들에서, 피로회복, 강장작용, 면역기능 강화 등의 많은 효능이 의학적으로 입증되어 널리 사용되고 있는 약용식물이다. 특히 인삼이 가지는 다양한 의학적 효능에 기여하는 인삼의 주요 약용성분으로 진세노사이드(ginsenoside)라는 화합물이 주목을 받고 있다.
그러나, 의약품으로써 진세노사이드의 활용 가능성이 점차 확대되고, 건강기능성 식품, 기능성 화장품 소재 등으로써의 수요도 높아지고 있는 추세지만, 전통적인 인삼의 재배방식은 비효율적일 뿐만 아니라 이를 통해서 얻을 수 있는 진세노사이드의 양은 매우 한정적이다. 따라서 진세노사이드의 고효율, 저비용 대량생산을 위해 재조합 효모 및 대사공학 기술을 이용한 진세노사이드 생산 세포공장 개발은 식물체로부터 추출해내는 기존의 고가의 복잡한 생산 공정을 대체할 수 있는 경제적인 생산 시스템을 제공할 것으로 기대되고 있다.
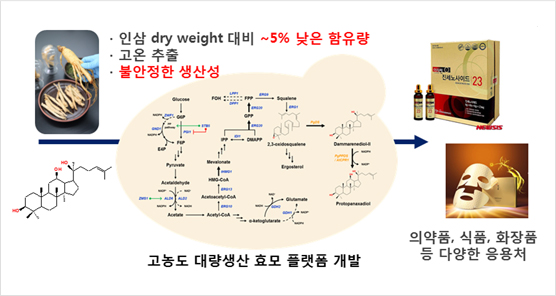
2. 연구내용
본 연구진은 효모의 조효소(NADPH) 생산과 관련된 세포 내 biosynthetic pathway 개량을 통해 진세노사이드 생산과정에서 필요한 조효소의 공급을 증가 시키고, 부수적으로 발생되는 oxidative stress를 감소시켜 진세노사이드 생산에 필요한 핵심 전구체, 즉 프로토파나사디올(protopanaxadiol, PPD)의 생산량을 증가시킨 효모를 개발하고자 하였다 (그림 1).
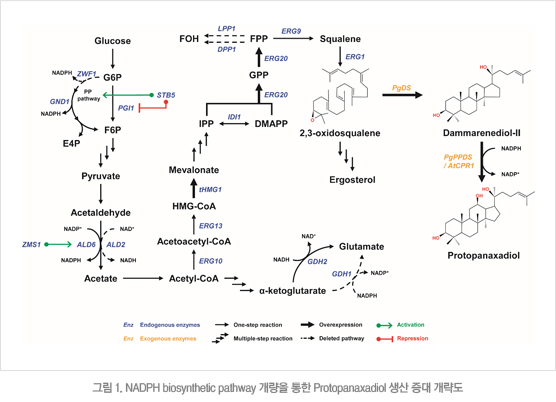
□ Protopanaxadiol 생산 효모 균주 제작
생산을 목표로 하는PPD는 다양한 형태의 진세노사이드 생합성에 필수적인 핵심 전구체로써, 효모 (Saccharomyces cerevisiae)를 생산 플랫폼으로 인삼 및 애기장대 (Arabidopsis thaliana) 유래의 유전자로 구성된 PPD 생산 대사경로를 도입 시킴으로써 포도당으로부터 PPD를 생산하는 효모 균주를 제작하였다. 외래 유전자로 구성된 PPD 생합성 경로는 포도당이mevalonate pathway를 통해 만들어지는 2,3-oxidosqualene 에서 시작된다. 인삼유래의 유전자인 PgDS와 PgPPDS, 애기장대 유래의 AtCPR1은 각각 GPD promoter와 함께 효모 내 유전체에 도입 되었다. 이와 더불어 PPD 생산에 필요한 전구체를 증가시키기 위해, 율속 반응(rate-limiting step)으로 알려져 있는 HMG1과 ERG20 유전자들의 활성 또는 발현을 강화 시킨 균주를 제작하였다. 구체적으로, Feedback inhibition으로 인해 활성이 저해되는 HMG1을 개량한 tHMG1(truncated HMG1)을 TEF1 promoter와 함께 도입하였으며, CCW12 promoter와 함께 ERG20 유전자를 추가 도입하여 PPD를 생산할 수 있는 효모 균주를 제작하였다. 이와 같이 제작된 균주는 144시간의 발효 이후 0.5 mg/L 정도의 PPD를 생산 하였다(Flask 수준 발효).
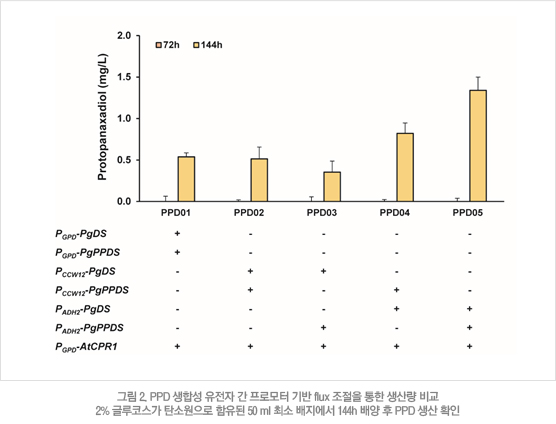
□ 프로모터 기반 Flux 조절을 통한 protopanaxadiol 생산량 증가
NADPH biosynthetic pathway 재설계에 앞서 효율적인 PPD생산에 필요한 대사흐름을 최적화 시키기 위해, 상이한 발현양상을 보이는 3 가지의 탄소원 의존형 프로모터에서 PgDS와 PgPPDS를 발현하는 균주를 제작하였다. 3가지 프로모터에는, 포도당에서 활성이 제일 강력한 GPD promoter, 에탄올에서 제일 활성이 강력한 ADH2 promoter, 그리고 탄소원 비의존성 CCW12 promoter가 사용되었다. 여러 조합의 프로모터를 사용하여 PgDS와 PgPPDS를 발현하는 균주들을 비교 해본 결과, 두 유전자 모두 에탄올에서 활성이 제일 강력한 ADH2 promoter를 사용하였을 때 가장 높은 PPD 생산량을 보였다 (그림 2b). GPD promoter를 이용해 제작된 기존 균주에 비해 약 2.5배 가량 높은 1.3 mg/L의 PPD 생산농도를 확인하였으며, 이러한 결과는 포도당을 이용한 효모 발효 과정에서 나오는 에탄올이 PPD 생산과 밀접한 관계에 있음을 시사한다.
□ 조효소(NADPH) 생산경로 재설계를 통한 protopanaxadiol 생산량 증가
NADPH는 PPD 생산경로의 마지막 단계인 PgPPDS에 의한 dammarenediol-II 전환에 필수적인 조효소 이다. NADPH biosynthesis pathway에 관련된 유전자 중 본 연구진은 NADPH를 사용하여 세포 성장에 필수적인 glutamate를 생성하는 효소 GDH1, NADH를 사용하여 glutamate를 생성하는 효소 GDH2, NADH를 생성하며 acetaldehyde를 acetate로 전환시키는 효소 ALD2, 같은 촉매작용에 NADPH를 생성하는 효소 ALD6, 효모에서 NADPH의 생산에 중추적인 역할을 하는 인산화 오탄당 경로의 핵심 효소 ZWF1, 세포 내의 산화스트레스에 반응하여 활성화되는 전사인자 STB5와 ZMS1을 이용하여 세포 내 NADPH의 농도를 높이고, 그에 따른 결과로써 PPD의 생산농도를 증가 시키고자 하였다 (그림 1).
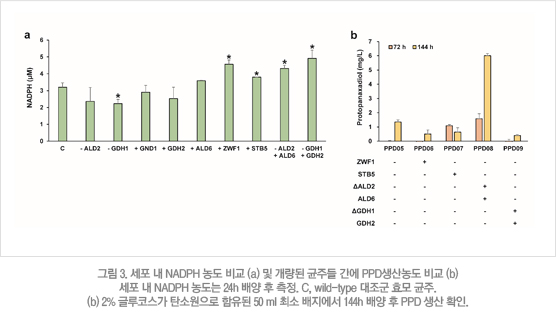
Isozyme 관계에 있는 단백질 중 NADPH를 생성하는 효소는 과발현 시키고, 반대로 사용하는 효소는 제거 시킴으로 세포 내 NADPH 양의 변화를 비교 하였다 (그림3a). 그 결과, 인산화 오탄당 경로에 관여하는 ZWF1, 전사인자 STB5, 아세테이스 생산경로에서 ALD2를 제거하고 ALD6를 과발현 시켰을 경우, glutamate 생산경로에서 GDH1을 제거하고 GDH2를 과별현 시켰을 경우 등에서 대조군 대비 통계적으로 유의한 NADPH 농도 증가를 보였다. 이렇게 선별된 유전자들을 PPD생산 균주에 적용시킨 결과, ALD2를 제거하고 ALD6를 과발현 시킨 균주에서 실제로 PPD 생산이 증가되어 6.01 mg/L의 PPD를 생산하였다 (그림 3b).
아세테이스 생산경로를 통한 NADPH의 농도 증가가 PPD 생산에 효과적으로 작용한 것에 착안하여, ALD6를 활성화 시킨다고 알려져 있는 전사인자인 ZMS1을 과발현 시킨 균주를 추가로 제작하였다. 또한, 유효한 target 유전자간에 시너지 효과(synergy effect)를 확인하고자 균주를 제작하였고, 균주들 간에 PPD 생산 농도, NADPH/NADP+ 농도, NADPH+NADP+ 농도들을 비교 하였다 (그림 4). 오탄당 인산화 경로로 소비되는 탄소원을 아세테이스 생산경로로 flux를 강화하여 PPD 생산농도를 높이고자, Glycolysis의 주요 side branch pathway인 ZWF1 유전자를 제거한 균주를 제작하였다. 그 결과, ZMS1을 과발현 시킨 균주에서 PPD 생산농도 증가를 확인 할 수 있었으나, ALD2를 제거하고 ALD6를 과발현 시킨 균주의 생산농도 보다 낮은 3.35 mg/L의 PPD를 생산하였다 (그림 4a). 즉, ZMS1과 ALD6 유전자간에 시너지 효과는 없음을 확인 하였다. ZWF1 유전자는 ALD6의 과발현이 선행된 균주에서 제거 되었을 경우에만 생산 농도 증가로 이어졌지만, 이 균주보다 낮은 5.66 mg/L의 PPD 생산 농도를 보였다.
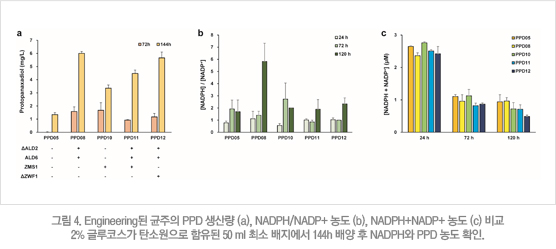
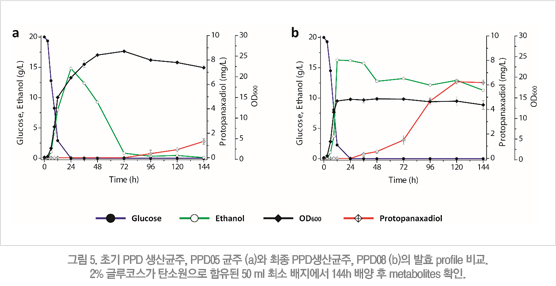
균주 내 NADPH/NADP+ 농도와 NADPH+NADP+ 농도를 비교 해본 결과에서 ALD2를 제거하고 ALD6를 과발현 시킨 균주에서 가장 높은 NADPH 농도를 보였으며, 이로부터 NADPH의 증가가 실제로 PPD생산 농도 증가로 이어졌음을 확인 할 수 있었다. 하지만, NADPH증가를 유도하는 여러 다른 target 유전자가 PPD생산에 큰 효과를 보이지 못한 것은, 개량하고자 하는 NADPH biosynthetic pathway가 PPD생산에 필요한 탄소원의 main carbon-flux pathway와 경쟁관계에 있었기 때문인 것으로 추정된다. NADPH 생산을 담당하는 ZWF1을 과발현 시킨 균주에서 NADPH의 절대적 농도는 증가했지만 PPD생산에는 효과가 없었고, 반대로 ZWF1을 제거한 균주에서 NADPH의 농도 증가는 두드러지지 않았지만 PPD 생산 증가에 효과적이었던 것은 PPD 생산으로의 대사유동성(metabolic flux)과 NADPH 농도 증가를 위한 재설계의 방향성이 일치해야 함을 시사한다. 본 연구를 통해 NADPH 생산경로를 재설계하는 전략으로, 초기 PPD생산 균주 대비 11배 이상의 PPD생산 농도를 보이는 균주 제작에 성공하였다. Flask 기반의 회분배양 결과, 기존 균주가 포도당 발효에 의해 만들어진 에탄올을 사용해서 성장하고 이와 경쟁 관계에 있는 PPD 생산 경로가 저해되어 최종 PPD생산 농도가 낮은 것에 비해, 개량된 균주는 축적된 에탄올을 PPD생산에 사용함으로써 최종 PPD 생산 농도가 크게 증가 했음을 확인 할 수 있다 (그림 5).
3. 연구의 성과 및 의의
본 연구에서는 NADPH 생산경로 재설계를 통해 진세노사이드 전구체인 PPD생산을 증가시킨 효모 균주를 개발하였다. 효모를 이용한 PPD 생산이 ethanol-growth phase와 밀접한 관계에 있음을 확인하였고, 또한 PPD생산에 필요한 탄소원의 main carbon-flux 강화가 PPD 생산에 중요한 역할을 하고 있음을 시사하였다. 조효소 생산경로 재설계를 비롯한 다양한 대사공학 기술을 적용시켜 최종적으로 6.01mg/L의 PPD를 생산 하였다. 본 연구에서 사용된 대사공학 기술은 포도당을 이용해 테르펜계의 다양한 고부가 바이오 물질을 만드는 바이오 플랫폼 기술에 적용되어 다양한 소재들을 보다 친환경적이고 경제적으로 생산하는데 기여할 것으로 기대한다.
참고문헌
1. Yu, T., Zhou, Y. J., Wenning, L., Liu, Q., Krivoruchko, A., Siewers, V., & David, F. (2017). Metabolic engineering of Saccharomyces cerevisiae for production of very long chain fatty acid-derived chemicals. Nature communications, 8, 15587.
2. Lee, J. Y., Kang, C. D., Lee, S. H., Park, Y. K., & Cho, K. M. (2015). Engineering cellular redox balance in Saccharomyces cerevisiae for improved production of L‐lactic acid. Biotechnology and bioengineering, 112(4), 751-758.
3. Partow, S., Hyland, P. B., & Mahadevan, R. (2017). Synthetic rescue couples NADPH generation to metabolite overproduction in Saccharomyces cerevisiae. Metabolic engineering, 43, 64-70.





