유전자 발현과 관련된 새로운 논리와 합성생물학적 가치
전남대학교 생물학과 이 진영, 김 근중 교수
1. 개요
합성생물학의 개념 도입과 이를 구현하기 위한 다양한 기술과 기법이 개발되어 유전자로부터 단백질이 발현되기까지 영향을 미치는 요인에 대해 보다 심도 있는 연구가 가능해졌다. 이러한 연구는 전형적인 방법으로는 구현할 수 없거나 제한된 수준에서 확인할 수 있었던 것들로, 공학적인 설계를 통한 수학적 모델링 및 통계분석 기법을 도입하여 유전자 서열에 따른 단백질 발현 정도를 예측하고 실제 발현양과 비교함으로써 관련된 변수를 찾는 것이다. 합성생물학은 이러한 변수를 찾는데 사용할 수 있는 다양한 유전적 도구를 제공할 뿐만 아니라 연구를 통해 밝혀진 새로운 논리를 실제 적용함으로써, 생물시스템의 유전자 발현과 조절에 관련된 근본적인 기작을 규명한 후, 이를 이용한 맞춤형 인공세포를 구현하는 것이 궁극적인 목표이다. 따라서 유전자 발현이나 조절 관련인자의 이해를 바탕으로 합리적인 설계를 통해 원하는 기능(성능)을 갖는 인공세포의 구현이 가능할 것이라는 기대를 가능하게 하는 것이다.
유전자 수준에서 단백질 발현에 영향을 미치는 대표적인 요소로는 promoter, RBS, transcription factor binding site, terminators, UTR, aptamer (riboswitch) 등이 있으며, 이들은 모두 목적 단백질의 발현조절을 위해 합성생물학적으로 재설계가 가능한 부분으로, 상기 요소 전체를 통합해 발현모듈이라 불리기도 한다. 기존의 연구들은 자연적으로 존재하는 이들 요소의 개별적 선별과정 후에, 특성을 분석하여 목적 유전자의 발현을 위한 도구로서 단순접목(incorporation)을 시도하였다. 합성생물학의 발달은 이들 자원이 지닌 특성을 개량하거나 목적에 맞게 변형하기 위한 합리적인 설계법과 도구를 제시하였다. 프로모터를 예로 들면 기존방법의 경우, 상대적으로 강한 세기를 갖는 프로모터 또는 약한 세기를 갖는 프로모터를 그대로 사용하거나, 조절인자와의 결합을 위해 operator 부분을 도입하여 활용하는 것이 일반적인 방법이었다. 하지만 최근 연구결과를 살펴보면 하나의 프로모터 서열로부터 프로모터 세기에 주요한 영향을 미치는 -35와 -10 주위의 spacer sequence 를 합성생물학적 방법으로 재설계하여 연속적인 다양한 세기를 갖도록 프로모터 라이브러리를 제작하고, 원하는 세기의 프로모터를 적소에 활용함으로써 꼭 필요한 수준의 단백질 발현이 이루어질 수 있도록 설계가 가능해졌음을 알 수 있다 (Hammer, et al. 2006). 뿐만 아니라 RBS calculator, UTR designer 와 같은 번역수준을 예측할 수 있는 프로그램을 활용하여 원하는 수준의 발현세기를 갖도록 관련요소를 설계할 수도 있다 (Salis 2011, Seo, et al. 2013).
발현모듈에 포함된 조절인자 (cis-acting factor)의 재설계 외에도 목적 단백질의 ORF 서열을 변형하여 발현양을 늘리는 방법도 주목을 받고 있다. 특히 난 발현되는 외래 유전자를 특정숙주에서 발현시키고자 할 때, 발현 숙주의 codon usage 정보를 기반으로 codon 을 최적화해 유전자를 합성하는 방법으로 단백질 발현수준을 조절할 수 있는 것으로 알려져 있다. 연구결과에 따르면 codon optimization 과정을 통해 재설계할 경우 동일한 일차구조를 갖는 단백질의 발현율이 250 배까지 차이가 날 수 있다고 알려져 있다 (Kudla, et al. 2009). 하지만 codon bias가 단백질의 발현양을 결정하는 결정적인 요소가 아니라 유전자 서열에 담겨있는 다양한 정보 (초기번역속도, 희귀코돈 분포, 전사체의 구조 및 안정성, 전사체의 구획화, UTR 과 같은 번역인자와의 결합부위)가 단백질 발현에 복합적으로 작용한다는 결과가 다양한 연구과정에서 보고되어, 이들을 통합적으로 조절하는 것이 중요할 수 있음을 시사하고 있는 것에 주목할 필요가 있다.
본 논고에서는 합성생물학적 방법으로 조절 가능한 단백질 발현에 관련된 인자들 중, 비교적 최근에 이론이 정립되었거나 제안된 새로운 논리와 관련하여 이들의 연구방법과 적용점에 대해 간략히 서술하고자 한다.
1. N-말단 codon bias 와 번역속도가 유전자 발현에 미치는 영향
생물은 하나의 아미노산을 지정하는 여러 종류의 codon 을 가지며, 종에 따라 codon usage 가 bias 되어 있어 외래 유전자의 발현에 큰 영향을 미친다. 대부분의 경우 숙주의 codon usage 와 유사한 배열 특성을 지닌 유전자가 발현에 유리하다고 알려져 있으나 예외도 존재하며, 최근에는 이러한 예외에 해당하는 이유가 무엇인지 여러 각도에서 연구가 진행 중이다. 명확한 이유는 알려져 있지 않지만, 다양한 생물종의 유전자 N-말단에는 rare codon 의 상대적인 빈도가 높은 경우가 많다 (Tuller, et al. 2010). 이러한 분포특성이 지닌 생리학적 의미를 규명하려는 노력의 결과로써, N-말단에 rare codon 의 비율이 높은 natural 유전자의 발현양이 상대적으로 높은 경우가 빈번한 것으로 알려져 있다. 이를 바탕으로 몇몇 연구에서는 유전자의 N-말단 rare codon 이 translation 초기 ribosome 의 elongation 속도를 늦추어 전체적인 translation efficiency 를 증가시킬 것으로 예상하였다 (Tuller, et al. 2010). 또 다른 논문에서는 N-말단의 rare codon 이 5’-UTR 을 포함한 mRNA의 이차구조 형성 정도를 약화시켜 단백질 발현에 중요한 영향을 미친다고 제안하였다 (Gu, et al. 2010). 두 이론 중에 어떤 이론이 단백질 발현에 보다 중요한 영향을 미치는지 확인하려면 많은 후속 연구가 필요하지만, 최근 연구보고에 따르면 약화된 RNA 의 2차 구조가 단백질 발현 증가에 좀 더 많은 영향을 미칠 수 있음이 제안되었다 (Goodman, et al. 2013).
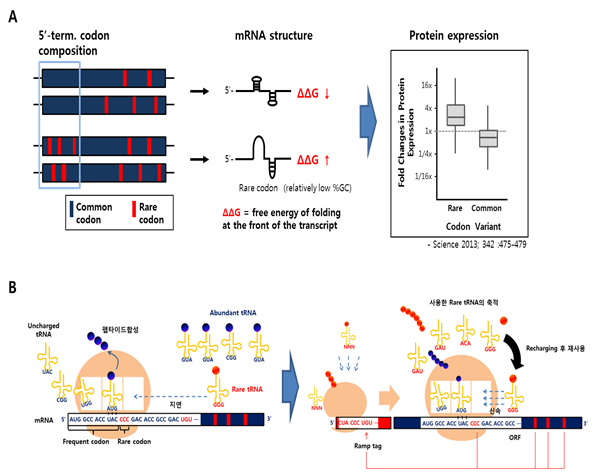
그림 1. N-말단 rare codon 의 유무와 단백질 발현 수준의 상관성 (A), 유전자의 앞 부분에 존재하는 rare codon 에 의해 모아진 tRNA 의 재사용을 통한 단백질 발현속도 유지원리 모식도 (B).
연구내용을 살펴보면, GFP 의 N-term 부위에 자연적으로 존재하는 다양한 codon 조합을 더하여 발현 수준을 비교하였을 때, 일반적으로 rare codon 을 갖는 GFP 가 common codon 을 갖는 GFP 에 비해 14배 이상의 높은 수준으로 발현된 것을 알 수 있으며, 이는 RBS 세기와 관계 없이 유지되는 특성인 것으로 나타났다 (그림 1A). 대장균의 rare codon 을 살펴보면 세 번째 염기에 A/T 가 주로 나타나는 것을 볼 수 있다. 결과적으로 A/T 가 좀더 약화된 RNA 구조를 형성하며, G/C 를 갖는 다른 synonymous codon 에서는 나타나지 않는 뚜렷한 발현 증가와의 상관관계를 확인하였다 (그림 1B).
이처럼 전사체의 구조는 유전자 발현에 많은 영향을 준다. 뿐만 아니라 유전자의 서열 정보는 번역시 elongation 속도를 늦추거나 일시적으로 멈춤으로써 (rare codon 에 의한 tRNA abundance와 관련) 단백질 발현에 큰 영향을 미친다. 특히 rare codon 이 유전자 내부에서 자주 나타날 경우, 리보솜의 elongation stalling을 유발하여 발현양을 극단적으로 떨어뜨리기도 한다. Codon bias 가 심한 이종숙주에서 외래유전자를 발현할 시 이러한 문제가 빈번하게 나타나며, 이를 해결하기 위해 codon optimization 방법이 도입되었다. 하지만 전체 서열을 대상으로 rare codon 을 치환하는 것은 경제적 측면에서 맞지 않을 뿐 아니라, 실제 기대만큼 효과가 나타나지 않는 경우가 빈번하게 관찰된다. 따라서 이러한 이론을 유전자 전체에 적용하기에는 문제가 있는 것으로 알려져 있다. 이를 보완할 수 있는 연구결과로써 다음과 같은 이론이 존재한다. 2010년 셀(Cell)에 보고된 가설에 따르면, 번역 과정 중 한번 사용된 tRNA는 단순히 유리되는 것이 아니라 ribosome 주위에 머무르며 aminoacyltransferase 에 의해 다시 충전되어 번역 중 재사용될 것으로 예측하였다 (Cannarozzi, et al. 2010). 따라서 N-말단에 rare codon 을 위치시키면 초기에 번역속도가 낮아 발현율의 저하가 예상되나, 이후에 나타나는 rare codon 에서는 초기에 recruit 된 rare codon tRNA 가 재사용됨으로 (그림 1C), 전체적인 단백질 발현에는 큰 문제가 없을 것으로 추정되었다. 실제 실험에서도 이러한 효과가 확인되어 짐으로써, 작은 DNA 조각 (tag 형태로 모아진 rare codon) 을 특정 유전자 앞에 위치시키거나 N-말단 부위를 deoptimize (commn codon 을 rare codon 으로 변경)하는 방법으로 외래 유전자의 발현을 조절할 수 있다는 새로운 발현 논리가 주목을 받고 있다.
합성생물학적 기법으로 새로운 요소들을 접목해 적용점을 넓히기 위해서는, 아직은 불확실하지만 새롭게 도입해야 할 다양한 변수 (약화된 전사체의 N-말단 구조, 가속 번역속도론, rare codon 분포와 tRNA 재사용)에 대한 심도 있는 이해는 반드시 필요한 선행과제이다. 앞으로의 연구는 이러한 이해를 바탕으로 유전자의 서열 (특히, N-말단 서열)을 합리적으로 설계하여 과발현의 유도는 물론, 발현된 단백질의 가용성과 활성을 원하는 수준으로 조절 가능한 규격화된 범용의 발현시스템을 구현하는 것이다.
2. 전사체의 subcellular localization
상기 보고에서처럼 N-말단을 coding 하는 전사체의 구조가 단백질 발현에 많은 영향을 미치며, 다른 연구결과에서 확인되었듯이 5’UTR과 3’UTR 또한 전사체의 안정성과 발현조절에 중요한 역할을 담당한다는 것은 주지의 사실이다. 한 예로 몇몇 유전자의 발현조절 방법으로 알려진 riboswitch는 주로 5’UTR 에 위치하며, 특정 기질에 반응하여 단백질의 번역을 전사체 수준에서 조절할 수 있다고 알려져 있다 (Garst, et al. 2011). 이러한 구조는 외부신호에 대한 빠른 대응과 tight regulation 이 가능한 조절 방법이며, 동시에 상호간섭이나 교란의 문제 (전사조절에 관여하는 프로모터가 지닌 단순한 sequence space 에서 생기는 문제) 를 피할 수 있다는 점에서 매우 중요한 의미를 갖는다. 유전자의 발현조절 과정에서 교란이나 상호간섭 문제를 회피하는 것은 생물이 한정적인 자원을 효율적으로 활용하는데 필수적이다. 따라서 정교한 (많은 check point를 지닌) 신호전달과정을 통해 trans-acting 을 하는 인자 (주로 단백질)와 cis-acting 을 하는 인자 (주로 염기서열)간의 상호작용을 효과적으로 조절하는 다양한 방법들이 생체에서 발견된다. 이러한 조절원리는 합성생물학 분야에서 전형적인 유전자 발현이 지닌 leaking 문제를 해결하고, 숙주시스템과의 비간섭에 의한 독립구동을 담보하여 유전자발현 효율을 재현성 있게 극대화하는데 꼭 필요한 전략이다.
진핵세포에서는 비간섭과 독립구동을 극대화하기 위해, 핵에서 생성된 전사체를 필요로 하는 각각의 세포 소기관으로 이동시켜 특정 반응 (또는 단백질 발현)이 필요한 곳에서 일어날 수 있도록 구획화되어 있다. 흥미로운 점은 전사체의 구획화와 발현조절에 전사체의 구조 (서열) 와 이와 관련된 RNPs (RNA-binding proteins)가 직접 관여한다는 것이다 (Weis, et al. 2013). 최근 연구 결과들에 따르면 원핵세포의 세포질도 진핵세포와 마찬가지로 고도로 구획화되어 있으며 (Lewis, et al. 2000), RNA 나 단백질 수준에서의 구획/집적화를 통해 유전자 발현에 중요한 영향을 미칠 것으로 예측되고 있다. 따라서 전사체의 서열정보가 일반적으로 예상할 수 있는 범위보다 폭 넓게 유전자 발현에 관여할 것으로 생각된다. 이를 뒷받침하는 하나의 증거로 2011년 Science 에 발표된 논문을 살펴보면, 대장균 세포막 안쪽에 고정된 단백질을 코딩하는 유전자의 전사체가 번역과는 무관 (translation independent) 하게 세포막 쪽으로 이동한다는 사실을 확인하고 실험적으로 증명하였다 (Nevo-Dinur, et al. 2011). 이는 기존의 전형적인 관점과는 다르게 아미노산 서열(signal peptide)이 아닌 전사체의 염기서열이 이동 (구획화를 위한)에 관여한다는 사실을 보여주는 매우 흥미로운 결과이다. 실험방법과 내용을 간략히 살펴보면 다음과 같다. 먼저 전사체의 subcellular localization 을 관찰하기 위한 도구로 phage MS2 coat protein binding sequence (6xbs) 와 이와 결합하는 MS2-GFP fusion 단백질을 리포터로 사용하였다. Cat (cytoplasmic chloramphenicol acetyltransferase) 과 LacY (membrane-bound lactose permease)를 암호화한 유전자의 upstream 에 6xbs 를 각각 클로닝한 후, 세포에서의 전사체 위치를 형광현미경으로 확인한 결과, cat 과 lacY 전사체가 단백질의 세포 내 위치와 동일하게 각각 세포질과 세포막 부위에 위치함을 확인하였다(그림 2A).
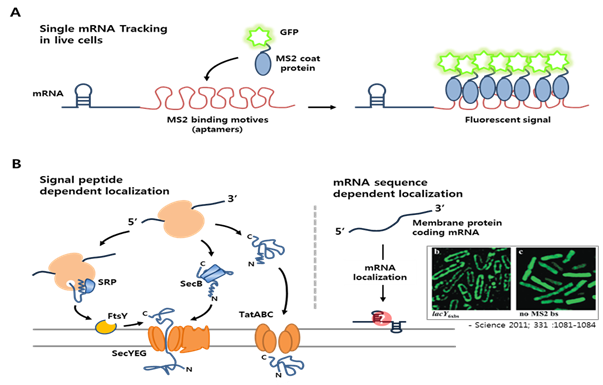
그림 2. 살아있는 박테리아에서 단일 mRNA 의 추적 방법 (A), signal peptide 의존적인 방법과 mRNA 서열(구조)에 의존적인 세포 내 이동 방법 (B)의 비교.
세포를 회수하여 세포질과 막을 분획한 뒤 cat 과 lacY 전사체 양을 정량하였을 때에도 동일한 결과를 확인할 수 있었다(그림 2B). 이후 실제 대장균의 bgl operon 을 대상으로 실험을 수행하였다. bgl operon 은 BglG (transcription factor), BglF (membrane bound sugar permease), BglB (soluble phospho-β-glucosidase) 로 구성되며, 일반적인 생리 환경에서 각각의 단백질의 세포내 위치가 다른 것으로 알려져 있다. 동일한 방법으로 실험한 결과, 각각의 단백질 위치와 전사체의 subcellular location 과의 상관관계를 확인하였으며, 특히 BglF 를 암호화한 전사체는 모든 조합에서 세포막에 위치하였다. BglF 전사체의 subcellular localization 이 translation independent 한지 확인하기 위해, ATG를 제거하거나 12개의 연속적인 rare codon을 삽입하여 단백질 번역을 제한한 경우에도, 전사체가 동일하게 세포막에 위치하는 것을 확인하였다. 또한 bglF 서열의 어느 부위가 membrane localization 에 관여하는지를 알기 위해 truncated bglF 서열을 이용하여 확인한 결과, membrane spanning domain 을 지정하는 서열에 전사체의 membrane targeting 정보가 있음을 확인하였다.
아직까지 박테리아에서 전사체의 subcellular localization 에 관한 정확한 원리는 밝혀지지 않았으나, 상기 연구 결과처럼 유전자 서열 자체에 세포 내 구획화에 관련된 정보가 내재되어 있음을 알 수 있다. 따라서 신호서열로서의 기능을 지닌 이러한 염기서열을 특정 유전자에 도입할 경우, 목적 유전자의 발현조절을 위한 새로운 기법으로 활용이 가능할 것으로 기대되어 진다. 세포 내 구획화는 발현 양을 결정하는 또 하나의 중요한 요소이기에 단밸질 과발현 유도에도 활용이 가능할 것이다. 합성생물학 관점에서 이러한 설계 요소와 이들을 활용할 수 있는 적용점을 찾는 것은 앞으로 매우 중요한 연구 과제가 될 것이다.
3. 분비 단백질의 유전자 서열이 발현에 미치는 영향
지금까지 발현에 관한 연구는 주로 세포질(cytoplasm)에서 기능하는 단백질들을 대상으로 이루어져왔다. 반면에 분비(secretion)되는 단백질 발현에 관한 연구는 상대적으로 부족한 실정이다. 또한 대부분의 연구는 단백질 수준에서 신호서열(signal peptide) 의 구조와 특성에 따른 분비경로와 발현수준을 규명하는데 그치고 있다. 박테리아에서 지금까지 알려진 단백질 분비경로는 총 8개(Type I~VI, Sec-SRP, Twin arginine targeting pathway)가 존재하며, 많은 종류의 단백질은 주로 Sec dependent pathway 를 통해 분비된다. 이들 경로를 통해 분비되는 단백질의 signal peptide의 구조를 살펴보면, 경로에 따라 조금씩 차이가 있지만 일반적으로 N-region, H-region, C-region 으로 구성된다. 이들을 구성하는 아미노산의 charge 와 hydrophobicity 가 각각 막으로의 이동과 membrane spanning strength 에 관여한다고 알려져 있다. 즉 단백질의 분비과정에서는 signal peptide 가 다른 어떤 요소보다 중요한 기능을 담당하는 것으로 알려져 있다. 하지만 signal peptide 서열을 분석해보면 cleavage site 앞의 ‘AXA’ 나 ‘RR’ motif (Tat-dependent signal peptide) 와 같은 단편적 특징 외에 서열상의 공통된 consensus를 찾기 어려우며, 따라서 실제 분비되는 모든 단백질의 분비 특성을 설명할 수 있는 정보로는 매우 부족한 것을 알 수 있다.
앞서 기술하였듯이 단백질이 기능하는 곳으로 전사체가 localization 될 수 있으며, 유전자 발현에도 관여할 수 있음이 제시되었다. 분비단백질도 이러한 방법으로 전사체가 분비경로로이동해 발현이 시작될 수 있을 것이다. 따라서 단백질의 signal peptide 서열 외에도 유전자 서열(염기) 정보가 분비에 영향을 미치는 요인으로 작용할 것으로 가정해 볼 수 있다. 최근의 몇몇 연구 결과는 이러한 논리를 뒷받침 한다. 한 예로 2014 년 Nature 자매지에 소개된 논문에 따르면, yeast 에서 분비단백질의 번역과정 중, SRP (signal recognition particle) 인식부위로부터 대략 35-40 codon 다음에 위치하는 nonoptimal codon cluster 에 의한 속도저하가 SRP 에 의한 인식(recognition)을 증가시켜 단백질 분비를 조절한다는 사실을 확인하였다 (Pechmann, et al. 2014).
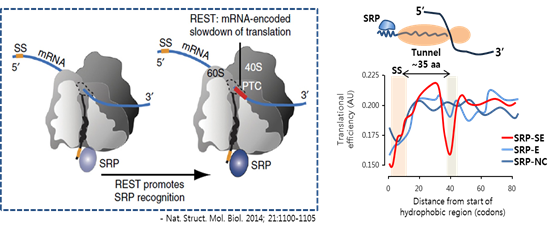
그림 3. 신호서열을 갖는 단백질을 코딩하는 유전자에 특정 위치에서 번역효율의 일시적 감소가 일어나는 REST 서열의 유무와 SRP enrichment(binding) 정도의 상관관계.
관련된 연구내용을 간단히 살펴보면 다음과 같다. 먼저 signal peptide 를 갖는 단백질을 in-vivo 에서 SRP enrichment 정도에 따라 SRP-E(enriched), SRP-SE(strongly enriched) 로 구분하고 signal peptide 의 hydrophobicity, putative binding motif, 특이서열의 패턴을 분석하여 SRP enrichment 와의 상관관계를 분석하였으나 관련 변수를 확인할 수 없었다. 반면에 mRNA 의 번역 효율의 일시적 감소가 나타날 수 있는 서열 정보가 동종에서 보존되어있는 것을 확인하였으며, 이들 서열이 SRP recruitment 에 중요한 역할을 할 것으로 생각하였다. 실제 SRP-E 와 SRP-NC(noncognate) 에서는 이들의 서열이 발견되지 않았으나 SRP-SE 에서는 SRP 인식부위로부터 ~38-43 codon 부위에 nonoptimal codon 이 위치함을 확인하였다 (그림 3). 따라서 이러한 서열을 REST (mRNA-Encoded Slowdown of Translation) 라 명명하고 transmembrane motif 를 지닌 다른 단백질을 coding 하는 유전자에서도 동일한 서열이 확인되는지를 분석하였다. 그 결과 다른 단백질의 경우에도, SRP 인식부위로부터 약 ~55 codon 부위에 이러한 기능을 지닌 구조적 특성이 나타남을 확인하였으며, 이 외에 서열정보도 동종에서 보존되어 있는 것을 확인하였다. 결과적으로 signal peptide 의 hydrophobic 한 서열이 SRP 의 결합에 영향을 미치나, 최소 임계 값을 초과한 경우에 hydrophobicity 의 증가는 더 이상의 SRP binding strength 를 높일 수 없으며, 반면에 전사체의 번역과정 중 REST 에 의한 local slow down 효과가 SRP를 recruitment 함을 증명하였다. 따라서 분비 단백질을 연구할 때 REST 와 같은 유전자 서열의 추가 혹은 대체를 통해 발현과 분비 효율을 조절할 수 있을 것으로 생각된다. 좀더 많은 case study 가 필요하겠지만, 합성생물학 분야에서 분비 단백질을 효율적으로 발현시키고자 할 때 이러한 요소를 접목하여 유전자를 설계함으로써 관련 연구에 활용할 수 있을 것으로 기대된다.
고찰
합성생물학의 발달과 omic 기반의 big data의 수집 및 분석방법의 개발, 그리고 다양한 연구 방법과 기술들이 개발되면서 유전자 발현에 관여하는 여러 변수에 관해 심도 있는 연구와 재해석이 이루어지고 있다. 특히 최근 몇몇 연구들을 통해 밝혀진 것처럼 유전자의 synonymous codon (숙주의 codon bias 와 함께) 이 갖는 의미는 기존에 우리가 상상했던 것보다 훨씬 많은 정보가 유전자에 내재되어 있음을 시사한다. 후속 연구를 통해 이와 관련된 발현/조절논리를 발견하고 확립하는 것이 매우 중요한 과제가 될 것이다. 현재 이루어지고 있는 유전자원 활용 방법은 특성이나 기능이 잘 알려진 소재 (part, 부품) 를 토대로 간단한 재설계와 재조합과정을 거쳐 구동원리를 설계한 후, 적용점을 찾는 수준의 연구가 주류를 이루어 왔다. 보다 많은 유전자원들에 대한 이해 (세포 생리적으로 내재된 발현/조절 원리)가 축적되고, 작동원리와 관련변수에 대한 공학적 설계가 가능해 진다면, 합성생물학의 궁극적 목표인 맞춤형 인공(공장)세포를 개발하는데 중요한 단초를 제공할 수 있을 것이다.
참고 문헌
1. Cannarozzi, G., N. N. Schraudolph, M. Faty, P. von Rohr, M. T. Friberg, A. C. Roth, P. Gonnet, G. Gonnet & Y. Barral (2010) A Role for Codon Order in Translation Dynamics (vol 141, pg 355, 2010). Cell, 141, 728-728.
2. Garst, A. D., A. L. Edwards & R. T. Batey (2011) Riboswitches: Structures and Mechanisms. Cold Spring Harbor Perspectives in Biology, 3.
3. Goodman, D. B., G. M. Church & S. Kosuri (2013) Causes and Effects of N-Terminal Codon Bias in Bacterial Genes. Science, 342, 475-479.
4. Gu, W., T. Zhou & C. O. Wilke (2010) A universal trend of reduced mRNA stability near the translation-initiation site in prokaryotes and eukaryotes. PLoS Comput Biol, 6, e1000664.
5. Hammer, K., I. Mijakovic & P. R. Jensen (2006) Synthetic promoter libraries - tuning of gene expression. Trends in Biotechnology, 24, 53-55.
6. Kudla, G., A. W. Murray, D. Tollervey & J. B. Plotkin (2009) Coding-Sequence Determinants of Gene Expression in Escherichia coli. Science, 324, 255-258.
7. Lewis, P. J., S. D. Thaker & J. Errington (2000) Compartmentalization of transcription and translation in Bacillus subtilis. Embo Journal, 19, 710-718.
8. Nevo-Dinur, K., A. Nussbaum-Shochat, S. Ben-Yehuda & O. Amster-Choder (2011) Translation-Independent Localization of mRNA in E. coli. Science, 331, 1081-1084.
9. Pechmann, S., J. W. Chartron & J. Frydman (2014) Local slowdown of translation by nonoptimal codons promotes nascent-chain recognition by SRP in vivo. Nature Structural & Molecular Biology, 21, 1100-1105.
10. Salis, H. M. (2011) The Ribosome Binding Site Calculator. Synthetic Biology, Pt B, 498, 19-42.
11. Seo, S. W., J. S. Yang, I. Kim, J. Yang, B. E. Min, S. Kim & G. Y. Jung (2013) Predictive design of mRNA translation initiation region to control prokaryotic translation efficiency. Metabolic Engineering, 15, 67-74.
12. Tuller, T., A. Carmi, K. Vestsigian, S. Navon, Y. Dorfan, J. Zaborske, T. Pan, O. Dahan, I. Furman & Y. Pilpel (2010) An Evolutionarily Conserved Mechanism for Controlling the Efficiency of Protein Translation. Cell, 141, 344-354.
13. Weis, B. L., E. Schleiff & W. Zerges (2013) Protein targeting to subcellular organelles via mRNA localization. Biochimica Et Biophysica Acta-Molecular Cell Research, 1833, 260-273.





